
É necessário ter muito cuidado com as ferramentas de terceiros que se utiliza para gerir a conta WhatsApp. A segurança da plataforma de mensagens mais popular do planeta foi novamente posta em causa, desta...



Deseja receber notificações?




É necessário ter muito cuidado com as ferramentas de terceiros que se utiliza para gerir a conta WhatsApp. A segurança da plataforma de mensagens mais popular do planeta foi novamente posta em causa, desta...

O consultor da UNESCO na área da educação mediática, Alexandre Sayad, admitiu, em entrevista à Lusa, que nenhum país está totalmente preparado para lidar com a desinformação.

Os dados da S&P Global Market Intelligence mostram forte apetite de private equity e hyperscalers, apesar das preocupações com avaliações elevadas e financiamento por dívida

A Agência Espanhola de Proteção de Dados (AEPD) alertou hoje que o TikTok continua a transferir dados pessoais dos utilizadores europeus para países terceiros, como a China, violando a regulamentação europeia.

A Agência Espanhola de Proteção de Dados (AEPD) alertou hoje que o TikTok continua a transferir dados pessoais dos utilizadores europeus para países terceiros, como a China, violando a regulamentação europeia.

A medida propõe que os utilizadores melhorem a experiência de utilização sem recorrer a hashtags genéricas.

Portugal e Espanha recebem novos espaços modernizados da Moeve, com serviços ampliados e uma das maiores redes de carregamento rápido da Península Ibérica.



ENTREVISTA || Cláudia Pina, é magistrada, integrou a Eurojust e escreveu um livro com o jornalista José Vegar onde explicam como o cibercrime evoluiu com a inteligência artificial, identifica as fraudes e ataques mais preocupantes e revela as tendências que vão marcar os próximos anos

🗞️ 7 notícias a não esquecer Sempre que há mudança de tecnologia, ou uma revolução tecnológica, as indústrias abalam. Aconteceu inúmeras vezes na história da humanidade, de que a passagem recente do analógico ao digital é só um exemplo. Muitas marcas analógicas não conseguiram assegurar com sucesso as transições tecnológicas e perderam terreno. Algumas até desapareceram. […] The post TOP of the WEEK: Entre ruturas tecnológicas e novas fortunas appeared first on Forbes Portugal.

A empresa de Mark Zuckerberg pretende que se subscreva uma assinatura do serviço “Meta Verified” para poder continuar a partilhar hiperligações. O valor da subscrição deverá variar conforme as funcionalidades escolhidas. Para já, o modelo avança como um teste, abrangendo apenas alguns utilizadores.

A associação que representa as empresas petrolíferas alertou esta quinta-feira que a reversão do desconto em vigor no Imposto sobre os Produtos Petrolíferos (ISP) incentiva práticas ilegais na importação de combustíveis, agravando distorções no mercado. Em comunicado, a Associação de Empresas Portuguesas de Combustíveis e Lubrificantes (EPCOL) manifesta “profunda preocupação com a persistência de práticas […]



O site Pornhub confirmou que sofreu um acesso não autorizado a dados de utilizadores, potencialmente afetando mais de 200 milhões de contas. O incidente foi atribuído ao grupo de hackers ocidental ShinyHunters, conhecido por ataques anteriores a grandes plataformas digitais.

Se o teu smartphone vibrou mais do que o habitual na manhã desta quinta-feira (18), não foste o único. Uma vaga repentina de queixas invadiu as redes sociais, com inúmeros utilizadores do Instagram a reportarem o recebimento excessivo de notificações sobre novos Stories, mesmo quando as definições da aplicação deveriam impedir tais alertas.O problema parece afetar perfis de forma aleatória, independentemente do sistema operativo, e tem gerado frustração pela falta de controlo sobre a funcionalidade.Uma ...

A CP recebeu hoje a primeira de 22 automotoras encomendadas à Stadler em 2020. A entrada em operação está prevista para o segundo semestre do próximo ano. The post CP recebeu a primeira automotora Stadler first appeared on Transportes & Negócios.

A relação entre as redes sociais e o conteúdo externo sempre foi tensa, com as plataformas a tentarem manter os utilizadores dentro das suas "muralhas" o máximo de tempo possível. Agora, a Meta parece estar a preparar-se para levar este conceito um passo mais longe no Facebook, testando um sistema que coloca a partilha de links externos atrás de uma barreira de pagamento para os criadores de conteúdo.Este movimento, se for implementado de forma alargada, poderá mudar radicalmente a forma como ...
A discussão sobre a inteligência artificial entrou finalmente no núcleo dos sistemas de gestão empresarial. Durante anos, o ERP (Enterprise Resource Planning) foi encarado como uma infraestrutura estável e imprescindível, mas pouco ágil na sua capacidade de adaptação. Hoje, esse diagnóstico já não descreve a realidade. A convergência entre IA, automação e análise avançada está […] The post A integração inteligente: Como a IA e automação estão a redefinir a competitividade das empresas appeared first on Forbes Portugal.


As redes sociais nunca mais vão ser as mesmas. Instagram vai avançar com mudança pioneira para os utilizadores.

O novo relatório "Kaspersky Security Bulletin 2025 Statistics" revela que a Inteligência Artificial marcará o panorama da cibersegurança em 2026, através de modelos de linguagem e inteligência generativa que irão melhorar as capacidades de proteção, mas também ampliar as possibilidades de ciberataques por parte dos cibercriminosos. O conteúdo Tecnocrónica: cibersegurança marca atualidade mas há mais aparece primeiro em Lidador Noticias.

A segurança dos utilizadores do WhatsApp está novamente sob ameaça devido a uma nova campanha de phishing batizada de GhostPairing. Este ataque, detetado pela equipa de investigação da Gen Digital, utiliza a funcionalidade legítima de emparelhamento de dispositivos para permitir que criminosos assumam o controlo total de conversas e ficheiros partilhados.Ao contrário de outros ataques que exigem a instalação de malware, o GhostPairing baseia-se em engenharia social para enganar a vítima. O objetivo ...

A cotação do barril de petróleo Brent para entrega em fevereiro terminou hoje no mercado de futuros de Londres em alta de 1,29%, para os 59,68 dólares, perante a perspetiva de os EUA bloquearem petroleiros venezuelanos.

A ideia surgiu de forma inesperada, durante uma escola de verão, em 2019, num centro de investigação internacional, dedicado à biologia e medicina espacial, reunindo estudantes e investigadores de várias áreas e países. Enquanto se discutiam missões de longa duração — como uma ida a Marte —, a conversa centrou-se nos riscos associados às mulheres […] O conteúdo Um grande passo para a humanidade: copos menstruais podem ser usados no espaço aparece primeiro em NiT.

Este ano que está prestes a terminar, os curadores, investigadores e associados científicos do Museu de História Natural de Londres descreveram um total de 262 novas espécies para a Ciência. O conteúdo Museu de História Natural de Londres descreve 262 novas espécies em 2025 também está disponível em Wilder.

A PandaDoc tem atualmente escritório em Lisboa, funcionando como um centro estratégico e operacional crucial, na Europa, para a empresa. Mas, o investimento da Indico também impulsionará a próxima fase de inovação em IA da PandaDoc, "aproveitando a vasta experiência da Índico Capital Partners em inteligência artificial e em promover a expansão de empresas".

A investigadora é a primeira mulher cientista e a primeira portuguesa a assumir este cargo na Academia Europeia de Microbiologia.

Depois de mais de três décadas de atividade, a iRobot, que criou os aspiradores robô Roomba, avançou com uma declaração de falência nos Estados Unidos. Num comunicado divulgado no domingo, a empresa anunciou uma “transação estratégica” que consiste numa aquisição pela chinesa Picea Robotics, a maior fabricante de componentes para os famosos aspiradores. “A Picea […]

Especialista em regulação digital diz que é consensual entre todos os Estados-Membros que haja uma proteção dos mais jovens da “invasão e lavagem cerebral que as redes sociais conseguem infligir”.

“Acreditamos mesmo que os dados têm que estar no centro de tudo que fazemos”, afirma Francisco Teixeira, country manager da WPP, em entrevista ao podcast do À Prova de Futuro. “É dar-lhe todo o protagonismo”. O grupo, que opera em mais de 100 países, utiliza dados e tecnologia como a inteligência artificial (IA) para ajudar […]

Portugal inclui-se no grupo de países que revelou disponibilidade para seguir o exemplo australiano.

Se acredita que as redes sociais refletem a opinião da sociedade, engana-se. O que vê não é o país, é o comportamento de uma "elite digital" que ocupa o espaço deixado livre pela maioria silenciosa.

Faz sentido que nos sintamos descansados com adolescentes que permanecem em casa, fechados nas redes, e nos alarmemos sempre que eles saem com amigos que os pais conhecem? É claro que não!

A plataforma online Reddit interpôs uma ação no Supremo Tribunal de Justiça australiano contra a nova lei do Governo que proíbe o acesso a menores de 16 aos às redes sociais.

De acordo com o Instituto Nacional de Estatística (INE), 79% dos portugueses utilizam redes sociais, o valor mais baixo desde 2017.

A Microsoft e a Amazon vão apostar forte em inteligência artificial (IA) na Índia.
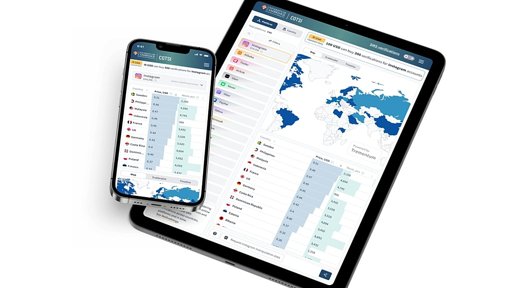
Novo índice da Universidade de Cambridge revela mercado clandestino com verificações falsas de contas nas redes sociais a 8 cêntimos, alimentando manipulação online e interferência eleitoral global.
Os pais estão felizes por voltarem a olhar os filhos nos olhos... para já.

Principais plataformas devem bloquear utilizadores menores de 16 anos ou enfrentar multas pesadas. Criadores relatam quedas repentinas no número de seguidores.

A Worten e a Rádio Popular confirmaram ao ECO que vão participar na segunda fase no programa dos vouchers do E-Lar, apesar de apontarem “desafios operacionais” e “pontos de melhoria” neste programa, que tem como objetivo promover a eficiência energética. “O programa representou um desafio operacional significativo para os retalhistas“, diz ao ECO Sofia Silva, […]

Um dia depois da proibição, vários adolescentes vangloriaram-se de continuar nas plataformas

O pai de uma criança de 15 anos afirmou temer que esta seja excluída na escola e do grupo de amigos por não conseguir utilizar a rede social

O prazo de submissão de candidaturas ao Concurso Estímulo ao Emprego Científico decorre de 15 de dezembro a 29 de janeiro de 2026.

Com esta medida, a Austrália torna-se no primeiro país a proibir o uso de redes sociais a menores

Pais que perderam os filhos em situações relacionadas com as redes sociais juntaram-se na residência oficial do primeiro-ministro para assinalar a entrada da lei em vigor

Empresas como a Meta, o YouTube ou o Tiktok arriscam penas de até 28,6 milhões de euros caso não cumpram.

A proibição, que entrou em vigor às 00:00 de quarta-feira, 10 de dezembro (hora local na Austrália, 13:00 de hoje em Lisboa), afeta pelo menos dez plataformas de redes sociais e 'streaming', entre as quais Facebook, Instagram, Threads, YouTube, TikTok, Snapchat, X, Reddit, Twitch e Kick.

Facebook, Instagram, Youtube ou TikTok estão entre as aplicações proibidas e a maioria delas garante que vai cumprir a lei

A Dinamarca planeia adotar a mesma medida no próximo ano.

Ricardo Araújo pretende estudar a origem evolutiva da endotermia, enquanto o projeto de Galego é no âmbito da neurociência

A Austrália tornou-se, esta terça-feira, o primeiro país do mundo a proibir oficialmente o acesso a menores de 16 anos a redes sociais, e já despertou a atenção de outros países, que ponderam adotar medidas semelhantes.

Lei entra em vigor no dia 10 de dezembro. TikTok vai aderir, Meta garante que se antecipou.

A Austrália tornou-se pioneira ao aprovar leis que obrigam as redes sociais a banir utilizadores com menos de 16 anos. A psicóloga Isa Silvestre analisa os prós e os contras da medida

Os portugueses concentraram as suas pesquisas em tecnologia, futebol e, em 2025, regressou a procura pelos locais de votos e resultados das eleições. O motor de busca Google voltou a fazer o ano em revista.

Já com um satélite da Constelação Lusíada no espaço e 12 a circular a órbita da Terra em “meados do próximo ano”, Ivo Vieira não quer que a constelação de satélites para comunicações marítimas da LusoSpace se fique por aqui. Em cinco anos, quer ter 50 satélites a orbitar a Terra. Neste momento, a empresa […]

A Austrália vai proibir o acesso de menores de 16 anos a uma série de plataformas e sites populares, incluindo o Facebook, Instagram, TikTok e YouTube, a partir de 10 de dezembro

Existem algumas evidências que apontam que o uso excessivo das redes sociais, principalmente nos adolescentes, pode estar a causar uma reconfiguração dos circuitos neuronais no sistema nervoso central
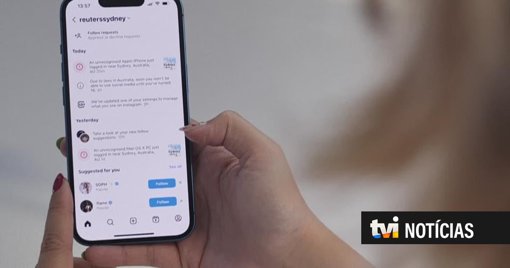
A Austrália é o primeiro país do mundo a criar leis que obrigam as redes sociais a banir menores de 16 anos. A medida obriga as empresas a manter um controlo apertado sobre quem usa as plataformas ou a sofrer pesadas multas. Entra em vigor no próximo dia 10 de dezembro.
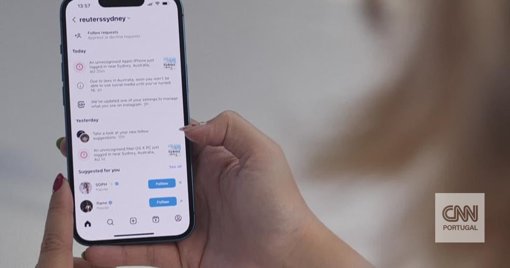
A Austrália é o primeiro país do mundo a criar leis que obrigam as redes sociais a banir menores de 16 anos. A medida obriga as empresas a manter um controlo apertado sobre quem usa as plataformas ou a sofrer pesadas multas. Entra em vigor no próximo dia 10 de dezembro.

Criou o Claude, é ativa no ecossistema, mas pouco se conhece. A Anthropic já contratou um escritório de advogados e estará a ter conversas informais para garantir injeção de capital.

Plataforma de 'streaming' de vídeos vai ser proibida no país a menores de 16 anos.

A Austrália vai proibir crianças com menos de 16 anos de usar redes sociais a partir do próximo mês

País vai proibir crianças com menos de 16 anos de usar redes sociais a partir do próximo mês.

Segundo o relatório "Ódio à venda - Como o Instagram permite que vendedores de mercadorias odiosas alcancem mil milhões de visualizações"

ONG salienta que existem plataformas de comércio eletrónico envolvidas na venda de mercadorias racistas promovidas na rede social.

Uma nova ferramenta do X que mostra a localização dos utilizadores está a expor inconsistências entre grandes contas russas e anti-UE, mas os investigadores avisam que os dados não são totalmente fiáveis.
Milhões de crianças criam contas nas redes sociais sem supervisão.

Uma conversa honesta sobre a vida pública e o trabalho nas redes: a pressão de aparecer, o burnout, a dificuldade de desligar e tudo o que ninguém vê por trás de ser criadora de conteúdos.

Ministra da Juventude reconhece que há benefícios em começar a discutir o tema a nvel nacional.

A ministra da Juventude, Margarida Balseiro Lopes, reconhece evidências científicas sobre os riscos da exposição às plataformas digitais e sublinhou que qualquer solução tem de envolver também as famílias

É uma questão de semântica: estudo defende que uso excessivo das redes sociais tende a ser hábito e não vício. Acreditar que é um vício leva a uma sensação de menor controlo e maior culpa.

Ian Anderson e Wendy Wood entrevistaram uma amostra aproximadamente representativa de 380 utilizadores norte-americanos do Instagram
Extensão de navegador com IA pode atenuar a reação de pessoas a opiniões políticas opostas, indica investigação focada nas presidenciais dos EUA de 2024

A maioria dos utilizadores das redes sociais considera que o uso excessivo deve-se ao hábito e não a um vício genuíno.

Para a maioria dos utilizadores das redes sociais, o uso excessivo se deve ao hábito, e não a um vício genuíno

O Parlamento Europeu quer interditar o acesso às redes sociais a adolescentes com menos de 16 anos.

Portugal e Espanha unem-se para apresentar parecer com recomendações.

A norma, aprovada com apoio bipartidário em 2024, bloqueia o acesso às redes sociais para crianças de 13 anos ou menos, e permite que adolescentes de 14 e 15 anos acedam a elas, mas com uma autorização dos pais ou tutores legais.

A saúde física e mental dos mais jovens está no centro das preocupações quanto ao uso excessivo da internet

O relatório pede mecanismos homogéneos de verificação da idade na União Europeia

Uma em cada três crianças portuguesas entre os 9 e os 11 anos acede à internet num smartphone "várias vezes ao dia", ficando duas horas por dia online (119 minutos), segundo o inquérito realizado em 19 países "EU Kids Online 2020"

O documento prevê que os menores possam aceder às redes sociais a partir dos 13 anos, mas apenas com o consentimento dos pais ou tutores legais

O Parlamento Europeu aprovou na quarta-feira uma proposta que apela à proibição das redes sociais para adolescentes com menos de 16 anos, enquanto os legisladores ponderam o seu impacto negativo na saúde mental e na política do debate online.

Governo avança com a decisão e lembra que que as três plataformas da Meta (Facebook, Instagram e Threads), bem como o Snapchat, o TikTok, o X e o YouTube devem tomar medidas para excluir utilizadores australianos com menos de 16 anos

O Parlamento Europeu também pediu à Comissão Europeia que exija a proibição de práticas nas redes sociais que induzam o vício nestas plataformas, e que sejam desativadas as predefinições nestas plataformas digitais que criam dependência, como o 'scroll' infinito

Mais de metade (54,7%) dos portugueses que usam redes sociais têm o hábito de seguir marcas e empresas nestas plataformas digitais, segundo o estudo “Os Portugueses e as Redes Sociais”, da Marktest, que realizou 801 entrevistas a indivíduos entre os 15 e os 64 anos entre os dias 3 e 15 de julho. A edição […]

Documento prevê que os menores possam aceder às redes sociais a partir dos 13 anos, mas apenas com o consentimento dos pais ou tutores legais

Documento revela que as principais plataformas digitais falharam na proteção dos menores em várias frentes.

O documento prevê que os menores possam aceder às redes sociais a partir dos 13 anos, mas apenas com o consentimento dos pais ou tutores legais.

O Parlamento Europeu (PE) aprovou hoje um relatório que pede uma idade mínima de 16 anos para aceder às redes sociais sem consentimento dos pais nos 27 países da União Europeia (UE) e mecanismos para cumprir esta regra.

Relatório aponta o dedo à ineficácia das estratégias que as gigantes tecnológicas têm vindo a implementar sobre conteúdos ilegais.

Uma semana de detox digital pode melhorar a saúde mental? Estudo indica: um em cada quatro jovens referiu menos sintomas depressivos após uma semana sem aplicações.

A posição está longe de gerar consenso entre os grupos políticos representados nos hemiciclos de Bruxelas e Estrasburgo

Os peticionários pedem um modelo semelhante ao "que está a ser implementado na Austrália", país que em dezembro deverá ficar na história como o primeiro do mundo a proibir o uso de redes sociais por parte de crianças com menos de 16 anos.

O Parlamento Europeu (PE) vai discutir um relatório que recomenda a proibição da utilização das redes sociais a menores de 13 anos e um limite mínimo de 16 anos, ainda que esta limitação esteja longe de reunir consenso. Os eurodeputados vão discutir durante o plenário desta terça-feira em Estrasburgo, em França, um relatório que aponta […]

Um grupo de pessoas lançou há um ano uma petição defendendo a proibição do uso de redes sociais a menores de 16 anos, recolheu mais de 12 mil assinaturas e entregou-a ao parlamento, onde continua "em apreciação".